[강세 토픽] 희귀질환 치료제 테마, 이수앱지스 +6.46%, 모아라이프플러스 +4.91%
증권플러스 | 2025.07.03 오후 12:17
[뉴스봇] 희귀질환 치료제 테마가 강세다. 전일 대비 2.2% 상승세이다. 이수앱지스 +6.46%, 모아라이프플러스 +4.91%, 압타바이오 +4.07% 등이 테마 상승을 이끌고 있다.
테마 설명
✔ 국내 기준 2만명 이하의 질병을 희귀질환으로 정의
✔ 일반의약품 대비 약가 5배↑..독과점 지위도 누릴 수 있어
✔ 글로벌 희귀의약품 시장 '28년까지 연평균 11% 성장 전망
희귀질환(Orphan disease, Rare disease)은 그 뜻이 의미하는 바와 같이 인구의 극히 일부가 앓고 있는 질환을 의미.
희귀질환에 대한 명확한 정의는 유병 인구 수로 정해지는데 그 기준은 국가별로 다름. 미국은 유병인구 20만명 이하, EU(유럽연합)는 18.5만명 이하, 일본은 5만명 이하, 한국은 2만명 이하인 질병을 희귀질환이라 정의. 이를 해당 국가의 전체 인구에 대한 비율을 이용하여 표준화하면 인구 10,000명 당 3~10명 수준.
현재까지 알려진 희귀질환은 7000~8000종에 달함. 이 중 80%가 유전질환이며 동일 질환이라 하더라도 환자들 간 증상이나 치료 반응의 편차가 심함.
절대적인 환자수인 인구의 7%를 기준으로 보면 한 자릿수 수준의 시장규모를 예측할 수 있음. 그러나 2016년 기준 희귀의약품은 전체 오리지널 의약품 시장의 16.5%를 차지. 환자 수보다 2배 이상 큰 시장 규모.
산업연구원에 따르면, 전 세계 희귀의약품 시장 규모는 2023년 1730억달러로, 2028년에는 연평균 11.6% 성장한 약 3000억달러에 이를 것으로 예측. 복제약과 희귀의약품을 제외한 전문의약품이 같은 기간 동안 9220억달러에서 1조2400억달러로 연평균 6.1% 성장하는 것과 비교하면 매우 빠른 속도로 성장. 전체 전문의약품 매출액 중 희귀의약품이 차지하는 비중도 2023년 14.8%에서 2028년 18.4%까지 성장할 전망.
희귀의약품은 일반의약품보다 약 5배 이상 약가가 높음. 반면 경쟁은 치열하지 않아 개발 시 독점적인 지위를 누릴 수 있는 장점. 정부는 개발을 유도하기 위한 ‘희귀의약품법’ 제정 등 제도적 측면을 이용해 인센티브 부여.
국내에선 희귀의약품으로 지정 시 조건부 허가제도를 통해 임상 2상을 마치고 우선 판매 허가를 받을 수 있음. 또한 시판허가를 받은 날로부터 4년 동안 독점권이 인정. 미국은 임상시험 승인·허가 기간 단축, 전문의약품 허가 신청비용 면제, 세금감면, 품목허가 취득 후 7년간 시장 판매 독점권 등 혜택이 있음.
정부는 의약품 개발을 장려하기 위해 2023년 3월 바이오헬스 신산업 규제혁신 방안을 통해 희귀질환 치료제로 대체 약제가 없으나 개선효과가 충분한 약제에 대해 ‘(식약처)품목허가-(심평원)급여평가-(건보공단)약가협상’ 병행 시범사업을 추진한다고 발표.
세계 각국도 희귀의약품 개발 장려를 위해 정책적으로 지원. 미국 식품의약국(FDA)은 희귀난치성 질환 치료제 개발을 촉진하기 위해 미국 인구 20만명 이하의 유병률을 가지는 질환을 대상으로 하는 약을 '희귀의약품(orphan drug, ODD)'로 지정해 심사 기간이 단축 및 임상비용 세액 공제, 신약 허가 심사비용 면제, 시판 후 미국 시장 7년 독점권 등의 혜택 부여. 유럽도 의약품 허가 관련한 프로토콜 지원이나 각종 비용 공제, 우선심사, 출시 후 10년간 유럽 시장 독점권 부여 등의 혜택존재.
-
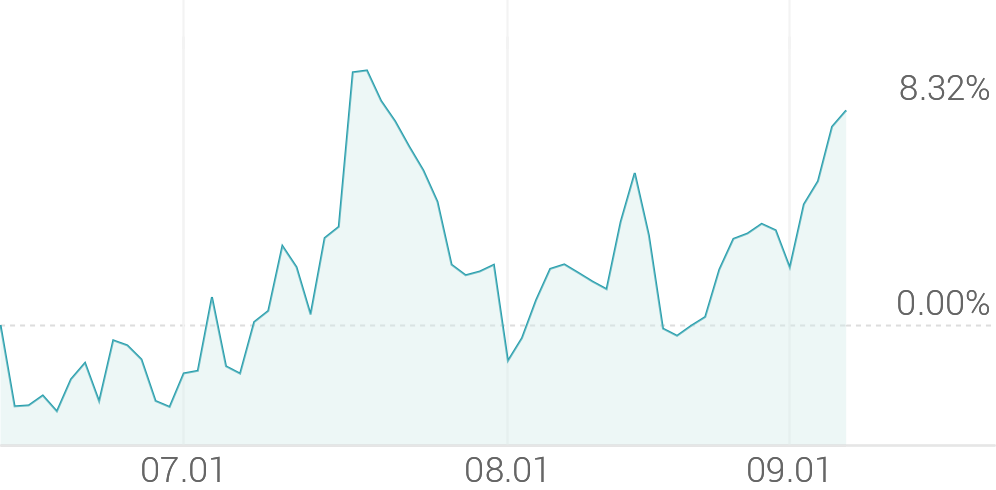
3개월 등락률
+26.05% -
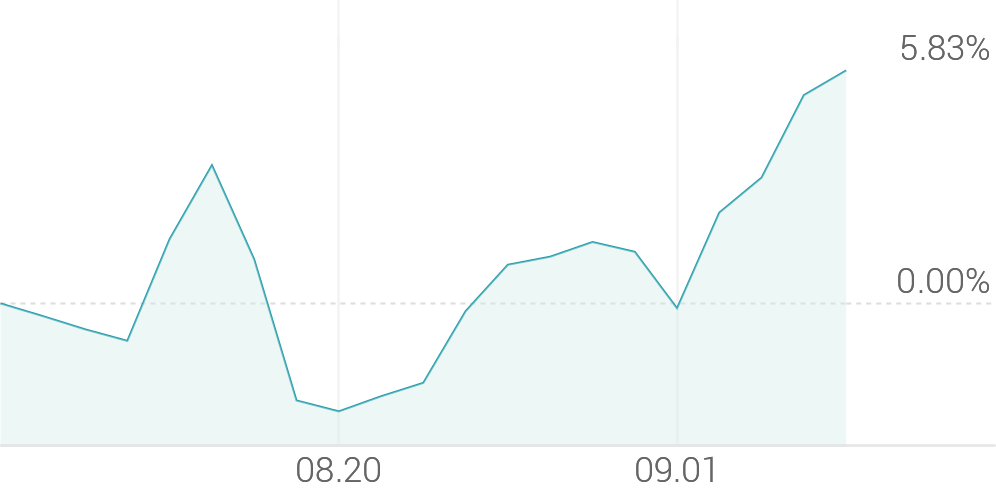
1개월 등락률
+4.97% -
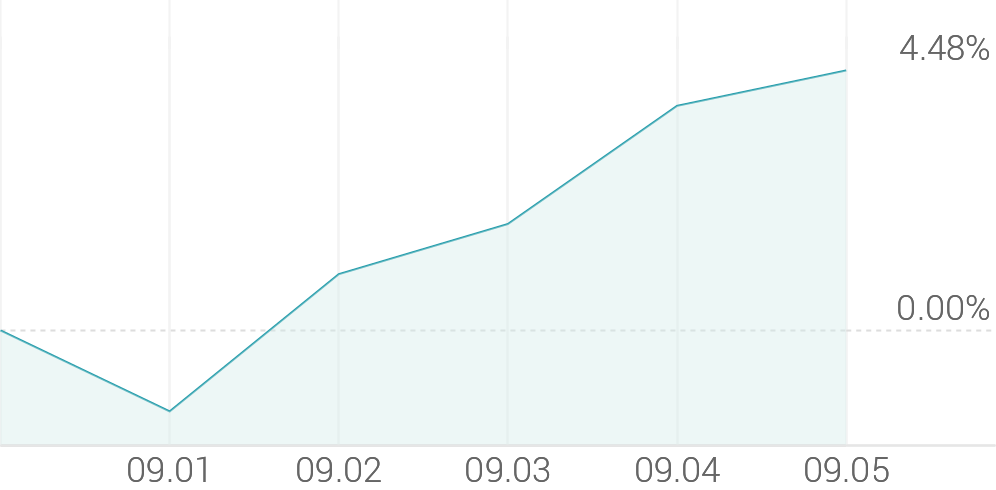
1주 등락률
+1.61%